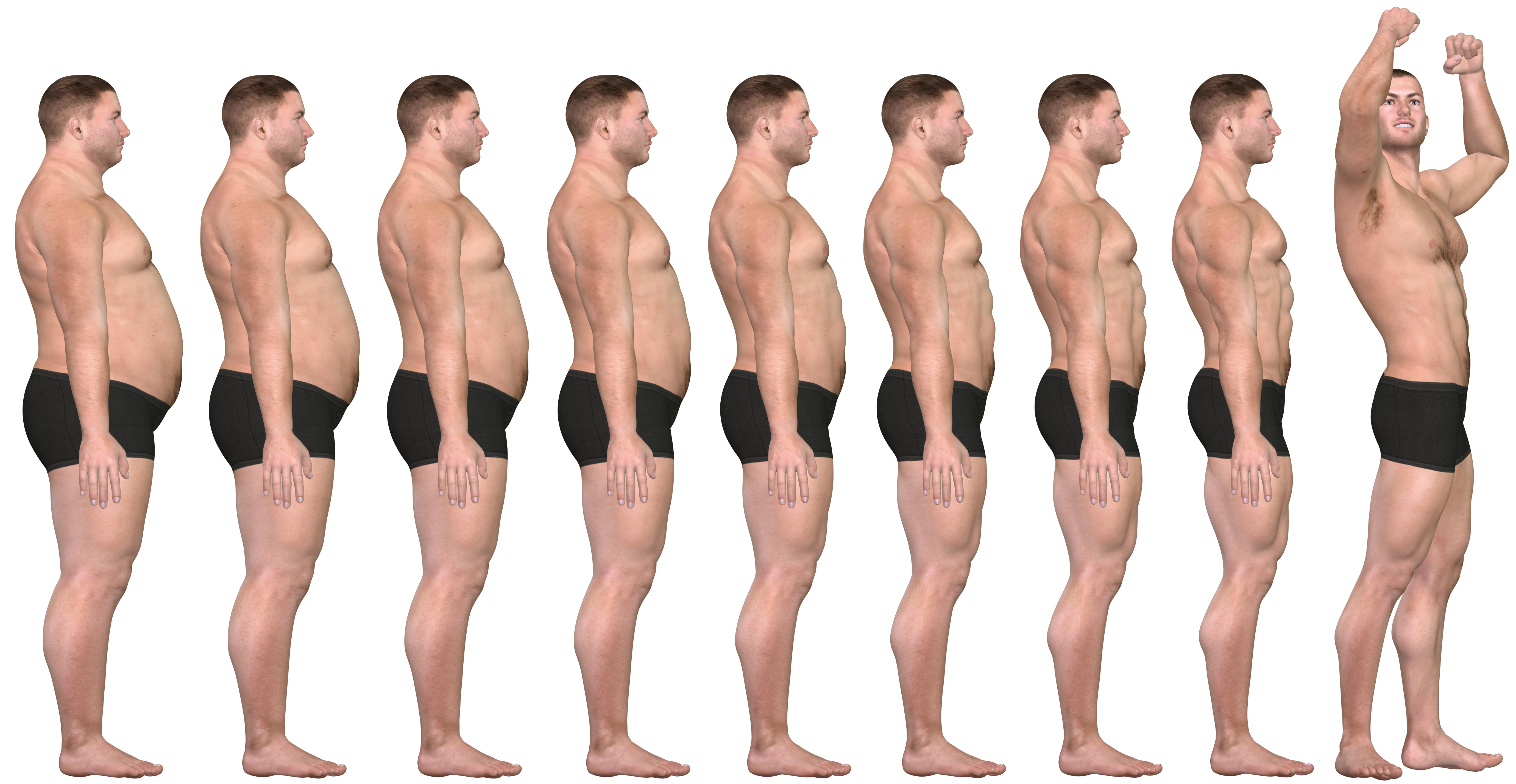
L’obesità e l’infertilità sono associate a una scarsa funzione sessuale.
Nell’uomo, il mantenimento dei livelli di testosterone è cruciale per lo stato di fertilità. Il legame tra obesità e carenza di testosterone è supportato da molti studi. I livelli di testosterone nei maschi obesi sono comunemente correlati a livelli simili a quelli degli uomini ipogonadici.
Negli uomini obesi, un aumento dell’attività dell’enzima aromatasi negli adipociti provoca la conversazione periferica del testosterone in estradiolo e una volta che i livelli di estradiolo aumentano, si osserva un feedback negativo sulla secrezione di LH, che porta alla soppressione dell’asse HPG e di conseguenza a una riduzione della produzione di testosterone da parte delle cellule di Leydig.
Gli adipociti sono i principali produttori di leptina e questo ormone di per sé influisce sull’LH e sul rilascio dell’ormone follicolo-stimolante (FSH) dall’ipofisi, alterando non solo l’ampiezza degli impulsi rilasciati, ma anche la pulsatilità; ciò influenza il bilanciamento dell’asse HPG in caso di eccesso di tessuto adiposo.
Studi più recenti hanno esplorato la connessione tra lo stress ossidativo e lo stato di fertilità degli uomini obesi. Lo stress ossidativo è una causa riconosciuta della disfunzione dello sperma poiché causa la perossidazione lipidica della membrana dello sperma, la frammentazione del DNA e aggrava l’apoptosi.
Per caratterizzare la popolazione di uomini affetti da ipogonadismo afferenti ad una clinica accademica di urologia si sono valutati i fattori di rischio per ipogonadismo primario vs secondario.
Gli uomini sono stati inclusi usando l’International Classification of Diseases-9, con i codici diagnostici R68.82 e 799.81 per bassa libido, 257.2 per ipofunzione testicolare ed E29.1. In base ai livelli di testosterone (T) e ormone luteinizzante (LH) i partecipanti sono stati identificati come ipogonadismo eugonadico, primario, secondario e compensato.
Tra i 231 uomini che avevano dosato entrambi i livelli di T e LH, il 7,4%, il 42,4% e il 7,4% erano classificati rispettivamente come ipogonadismo primario, secondario e compensato.
Solo un elevato BMI è stato associato con ipogonadismo secondario rispetto agli uomini eugonadici.
BMI, età, comorbilità, fumo o consumo di alcol non sembravano predire la diagnosi di ipogonadismo secondario.
La sindrome metabolica (MetS) rappresenta un insieme di condizioni che hanno un impatto negativo sulla salute umana in generale. La sua prevalenza è aumentata rapidamente e ha coinciso con una diminuzione globale dei tassi di natalità e del potenziale di fertilità.
Una recensione recentissima affronta questa osservazione attraverso lo studio della relazione tra MetS e la salute riproduttiva maschile.
Esaminando gli effetti dell’obesità, della dislipidemia, dell’ipertensione e dell’insulino-resistenza sulla fertilità maschile sono state descritte prove a supporto che spiegano la fisiopatologia della disfunzione dello sperma con ogni componente di MetS.
La disregolazione del sistema endocrino, l’innalzamento della temperatura scrotale, lo stress ossidativo e l’alterazione delle funzioni erettili ed eiaculatorie sono ben note conseguenze di MetS che possono compromettere la produzione e la funzione dello sperma, influenzando in ultima analisi la fertilità maschile.
Uno stile di vita sano caratterizzato da una buona alimentazione e un’attività fisica regolare è la chiave per prevenire gli effetti indesiderati di MetS non solo sulla fecondità, ma anche sulla salute e sul benessere generale.
E le donne?
Un intervento sullo stile di vita nelle donne con obesità e infertilità riduce il peso e migliora la salute cardiometabolica e la qualità della vita, che possono influire positivamente sulla funzione sessuale. Uno studio olandese di qualche anno fa ha valutato il costo e gli effetti di un programma di stile di vita strutturato di sei mesi mirato alla riduzione del peso seguito da cure convenzionali di fertilità (gruppo di intervento) rispetto alla sola terapia di fertilità convenzionale (gruppo di controllo) nelle donne sovrappeso e obese.
Ora i ricercatori riportano i risultati sulla funzione sessuale 5 anni dopo la randomizzazione.
Sono state randomizzate 577 donne, tra i 18-39 anni di età, con infertilità e un BMI ≥29 kg / m2, a un intervento sullo stile di vita di sei mesi mirato all’attività fisica, alla dieta e alla modificazione del comportamento oppure alla cura dell’infertilità in modo tradizionale.
La frequenza del rapporto sessuale e la funzione sessuale sono state valutate con il questionario di sessualità femminile McCoy (MFSQ), 5,4 ± 0,8 anni dopo la randomizzazione. I risultati sono stati aggiustati per la durata dell’infertilità, la sindrome dell’ovaio policistico e se le donne stavano tentando di concepire.
Il gruppo di intervento ha riferito più spesso di aver avuto rapporti nelle ultime 4 settimane rispetto al gruppo di controllo. Tra le donne che segnalano il rapporto nelle ultime 4 settimane, il gruppo di intervento (n = 75) ha avuto un rapporto più frequente e punteggi più alti per la lubrificazione vaginale e guadagnava un punteggio totale “funzione sessuale” più alto rispetto al gruppo di controllo (n = 72).
L’effetto dell’intervento sulla funzione sessuale era del 21% mediato dal cambiamento nell’attività fisica da moderata a vigorosa.
fonte:Ds nutrition